什么是“踢杀”疗法?这要从抗逆转录病毒疗法(ART)无法治愈HIV感染的主要原因谈起。
在HIV感染患者体内的一些细胞中,长期持续存在“潜伏”的HIV,这些病毒不表达病毒蛋白,被其感染的细胞因而无法被免疫系统识别。但一旦停药,病毒便会再次大量复制。
“踢杀”(kick and kill)疗法正是为了彻底清除这些潜伏病毒:先“踢出”这些病毒——诱导潜伏的HIV进行转录复制、表达蛋白(抗原),使其能够被免疫系统识别;然后一举将这些病毒“杀伤”——通过药物增强T细胞活性,识别并杀死这些储存有潜伏病毒的细胞。
此次发表的是一项名为“RIVER”的2期、开放标签、随机对照试验。试验在英国6家临床中心开展,纳入了60名患者,这些患者在过去6个月内被诊断为HIV阳性,且确诊后1个月内启动了ART治疗。患者1:1随机分组,仅接受ART治疗,或ART联用“踢杀”疗法。“踢出”剂是可以促使病毒转录的伏立诺他(vorinostat),“杀伤”剂是T细胞诱导疫苗,疫苗病毒载体是编码HIV序列但无法复制的病毒治愈艾滋病治愈艾滋病,从而可增加T细胞对HIV的针对性杀伤力。
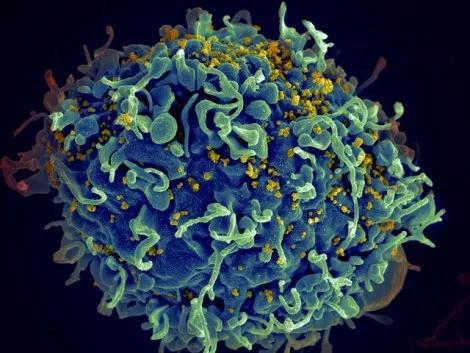
▲HIV(黄色颗粒)感染表达CD4的免疫T细胞(图片来源:NIH)
所有60名受试者都完成了研究和随访。研究人员测量了他们在治疗第16和18周后外周血CD4+ T细胞中分离出的HIV DNA总量,也就是大致测算“潜伏病毒的储存量”来评估疗效。HIV在CD4细胞中进行复制并进而破坏该细胞,此前研究也已表明,在HIV感染后不久,CD4+ T细胞中就会持续储存潜伏病毒。
总的来说,在两次检测中,ART联用“踢杀”疗法组和对照组的病毒DNA水平都没有统计学上的显著差别。虽然这有些令人遗憾,但研究人员确实观察到,“踢出”和 “杀伤”这两步的药物治疗后,患者体内有了一定变化。比如,接种疫苗后,患者的特异性T细胞反应增加;伏立诺他治疗的2小时内,组蛋白乙酰化也增加了,这提示病毒被激活。同时,试验也支持了“踢杀”疗法的安全性,两组都没有出现严重不良反应。
![▲治疗第9周和第12周时,ART+“踢杀”疗法组的患者,体内HIV特异性的T细胞占比显著更高(图片来源:参考资料[1])](https://img.jzka.cn/uploads/allimg/20230131/106f47be0fe2a1754aaf027b93e45785_4.png)
▲治疗第9周和第12周时,ART+“踢杀”疗法组的患者,体内HIV特异性的T细胞占比显著更高(图片来源:参考资料[1])
那么,为何没有达到的预期整体疗效?作者和一些专家评论都做出了谨慎解读,认为这未必意味着“踢杀”原理是错的,反而带来了新的启发和探索方向。
在《柳叶刀》同期刊发的评论中,墨尔本大学(The University of Melbourne)感染与免疫研究所主任Sharon Lewin教授指出了影响疗效的几点潜在原因:
首先,判断HIV存在情况,具有临床意义的唯一指标是ART停药后的反弹时间,而这项试验并未衡量这一点。试验中疗效的主要评估指标是HIV DNA总量,但其与ART停药后病毒反弹的关联,在不同研究中并不是特别一致。
其次,试验中没有观察到相关HIV RNA的明显增加,承担“踢出”角色的药物伏立诺他可能没有发挥足够的作用。一方面,试验中在应用“踢杀”疗法的同时,ART并未停药,这可能影响了对“踢杀”疗法的评估;另一方面,也可能是因为试验中的用药剂量低于既往研究,或患者选择就不合适——关于这点,Alex Nowbar女士也在BMJ评论中指出,这些都是新确诊患者,相较于长期感染者,对疗法的敏感性可能不同。
此外,试验启动于数年前,而随着科学发展,如今我们有了更多新武器可以用于“踢杀”疗法。试验中用的伏立诺他是一款“老药”,十年前就尝试用于抗艾治疗的临床试验,近年来已有多款潜在效力更有优势的“潜伏病毒逆转剂”。同时,现在已有指南共识支持谨慎停药,以探索不同的用药方案。